द्रव्याचे मोजमाप स्वाध्याय इयत्ता नववी विज्ञान आणि तंत्रज्ञान

1. उदाहरणे लिहा.
अ. धन आयन
उत्तर :
i) सोडिअम आयन (Na+)
ii) सिल्व्हर आयन (Ag+)
iii) क्युप्रिक आयन (Cu2+)
iv) पोटॅशिअम (K+)
आ. आम्लारिधर्मी मूलके
उत्तर :
i) पोटॅशिअम (K+)
ii) सिल्व्हर आयन (Ag+)
iii) अमोनिअम आयन (NH4+)
iv) कॅल्शिअम आयन (Ca2+)
इ. संयुक्त मूलके
उत्तर :
i) अमोनिअम आयन (NH4+)
ii) अमोनिअम आयन (NO3–)
iii) सल्फेट आयन (SO42-)
iv) फॉस्फेट आयन (PO43-)
ई. परिवर्ती संयुजा असलेले धातू
उत्तर :
i) तांबे
ii) पारा
iii) लोह
iv) टीन
उ. द्वि-संयुजी आम्लधर्मी मूलके
उत्तर :
i) सल्फेट आयन (SO42-)
ii) कार्बोनेट आयन (CO32-)
iii) डायक्रोमेट आयन (Cr2O72-)
iv) सल्फाइड आयन (S2-)
ऊ. त्रि-संयुजी आम्लारिधर्मी मूलके
उत्तर :
i) फेरिक आयन (Fe3+)
ii) क्रोमिअम आयन (Cr3+)
iii) अँल्युमिनिअम आयन (Al3+)
iv) गॅलिअम आयन (Ga3+)
2. खालील मूलद्रव्ये व त्यांच्यापासून मिळणाऱ्या मूलकांच्या संज्ञा लिहून मूलकांवरील प्रभार दर्शवा.
पारा, पोटॅशियम, नायट्रोजन, तांबे, कार्बन, सल्फर, क्लोरिन, ऑक्सिजन
उत्तर :
| मूलद्रव्ये | मूलकांच्या संज्ञा | प्रभार |
|---|---|---|
| पारा | Hg | Hg2+ |
| पोटॅशिअम | K | K+ |
| नायट्रोजन | N | N3- |
| तांबे | Cu | Cu2+ |
| कार्बन | C | C+ |
| सल्फर | S | S2- |
| क्लोरीन | Cl | Cl– |
| ऑक्सिजन | O | O2- |
3. खालील संयुगांची रासायनिक सूत्रे तयार करण्याच्या पायऱ्या लिहा.
सोडिअम सल्फेट, पोटॅशिअम नायट्रेट, फेरिक फॉस्फेट, कॅल्शिअम ऑक्साईड, अँल्युमिनिअम हायडॉक्साइड
उत्तर :
1) सोडिअम सल्फेट
उत्तर :

2) पोटॅशिअम नायट्रेट
उत्तर :

3) फेरिक फॉस्फेट
उत्तर :

4) कॅल्शिअम ऑक्साईड
उत्तर :

5) अँल्युमिनिअम हायडॉक्साइड
उत्तर :

4. खालील प्रश्नांची उत्तरे स्पष्टीकरणासह लिहा.
अ. सोडिअम ही मूलद्रव्य एकसंयुजी कसे आहे ?
उत्तर :
i) मूलद्रव्याच्या संयोग पावण्याच्या क्षमतेला संयुजा म्हणतात.
ii) सोडिअमचे इलेक्ट्रॉन संरूपण (2,8,1) आहे. म्हणजेच सोडिअम अणूच्या बाह्यतम कक्षेत 1 इलेक्ट्रॉन असतो.
iii) अष्टक पूर्ण करण्यासाठी रासायनिक अभिक्रियेदरम्यान सोडिअम एक इलेक्ट्रॉन देतो. यामुळे, धनप्रभारित सोडिअम आयन तयार होतो. म्हणून, सोडिअम हे एकसंयुजी मूलद्रव्य आहे.
आ. M हा दविसंयुजी धातू आहे. सल्फेट आणि फॉस्फेट मूलकांबरोबर त्याने तयार केलेल्या संयुगांची रासायनिक सूत्रे शोधण्यातील पायऱ्या लिहा.
उत्तर :
M हा द्विसंयुजी धातू आहे.
1) M या धातूचे सन्फेट या मूलकाबरोबर तयार होणाऱ्या संयुगाचे रासायनिक सूत्र लिहिण्याच्या पायऱ्या पुढीलप्रमाणे :

2) M या धातूचे फॉस्फेट या मूलकाबरोबर तयार होणाऱ्या संयुगाचे रासायनिक सूत्र लिहिण्याच्या पायऱ्या पुढीलप्रमाणे :

इ. अणुवस्तुमानासाठी संदर्भ अणूची आवश्यकता स्पष्ट करा. दोन संदर्भअणूंची माहिती द्या.
उत्तर :
i) अणू हे अतिशय सूक्ष्म असतात, त्यामुळे अणुवस्तुमान अचूकपणे मोजणे शक्य नसते. म्हणून अणूचे सापेक्ष वस्तुमान ही संकल्पना वापरली जाते. अणूचे सापेक्ष वस्तुमान मोजण्यासाठी एका संदर्भ अणूची गरज असते.
ii) हायड्रोजनचा अणू सर्वात हलका असल्याने सुरुवातीच्या काळात हायड्रोजनची निवड संदर्भ अणू म्हणून झाली. हायड्रोजनच्या केंद्रकात केवळ एक प्रोटॉन आहे म्हणून हायड्रोजन अणूचे सापेक्ष वस्तुमान 1 स्वीकारण्यात आले.
iii) दुसरा संदर्भ अणू म्हणून कार्बन होय. या मापनश्रेणीत कार्बनच्या एका अणूचे सापेक्ष वस्तुमान 12 स्वीकारले गेले. कार्बन अणूच्या तुलनेत हायड्रोजनच्या एका अणूचे सापेक्षवस्तुमान 12 X 1/12 म्हणजेच 1 असे ठरते.
ई. ‘अणूचे एकीकृत वस्तुमान’ म्हणजे काय ?
उत्तर :
i) ‘अणूचे एकीकृत वस्तुमान’ हे अणूचे किंवा रेणूचे वस्तुमान मोजण्यासाठी वापरले जाणारे प्रमाण एकक आहे.
ii) या एककाला ‘डाल्टन’ असे म्हणतात. यासाठी ‘u’ ही संज्ञा वापरली जाते. आणि 1 u = 1.6605 X 10-27 kg.
उ. पदार्थाचा मोल म्हणजे काय ते उदाहरणासहित स्पष्ट करा.
उत्तर :
i) संयुगाचा 1 मोल म्हणजे संयुगाच्या रेणूवस्तुमानाएवढे मूल्य असलेले ग्रॅममधील वस्तुमान होय.
ii) कोणत्याही पदार्थाच्या एक मोल राशीमधील रेणूंची संख्या निश्चित असते. कोणत्याही पदार्थाचा एक मोल म्हणजे त्या पदार्थाचे 6.022 X 1023 रेणू होय.
उदा :
a) पाण्याचे रेणुवस्तुमान 18 u आहे म्हणून 18 ग्रॅम पाणी म्हणजे 1 मोल पाणी होय, यात 6.022 X 1023 पाण्याचे रेणू असतात.
b) कार्बन डायऑक्साइडचे रेणुवस्तुमान 44 u आहे म्हणून 44 ग्रॅम कार्बन डायऑक्साइड म्हणजे 1 मोल कार्बन डायऑक्साइड होय, यात कार्बन डायऑक्साइडचे 6.022 X 1023 रेणू असतात.
5. खालील संयुगांची नावे लिहा व रेणुवस्तुमाने काढा.
Na2SO4, K2CO3, CO2, MgCl2, NaOH, AlPO4, NaHCO3
उत्तर :
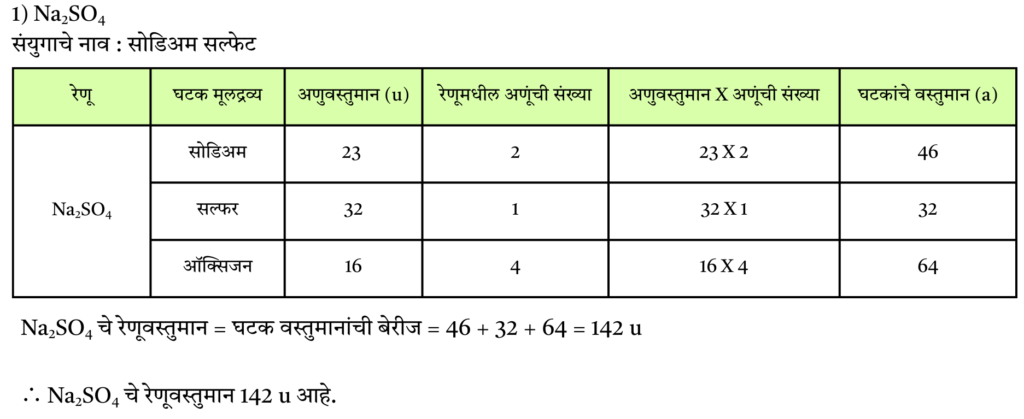
1) Na2SO4
उत्तर :
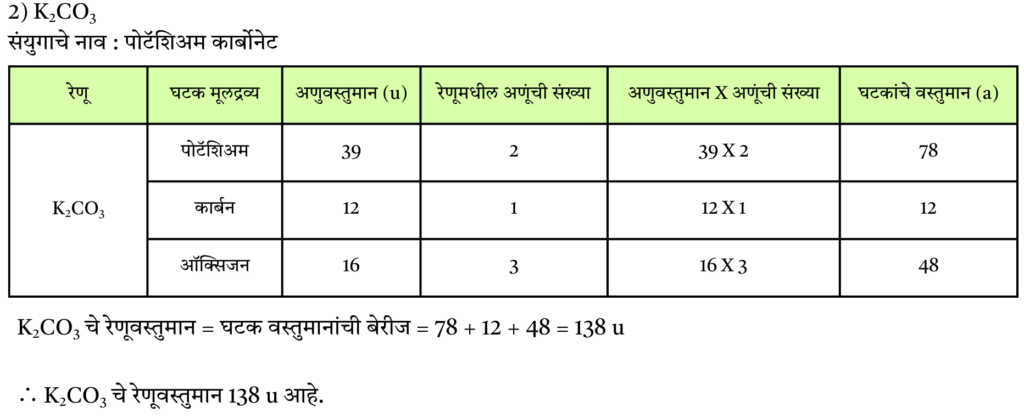
2) K2CO3
उत्तर :
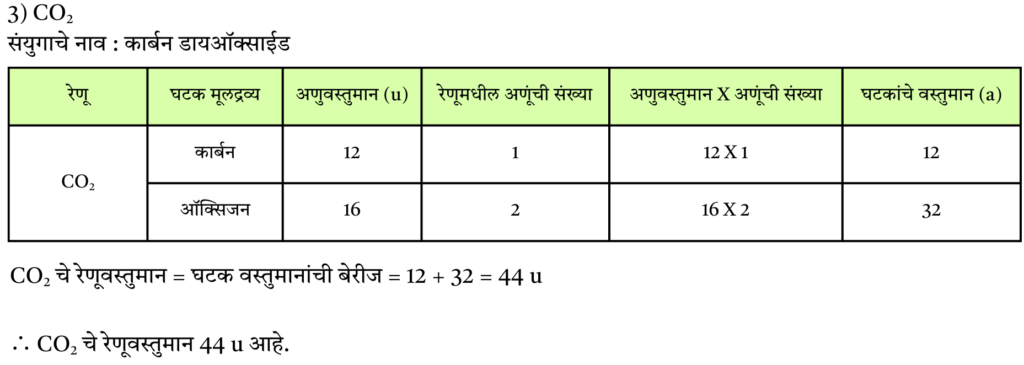
3) CO2
उत्तर :
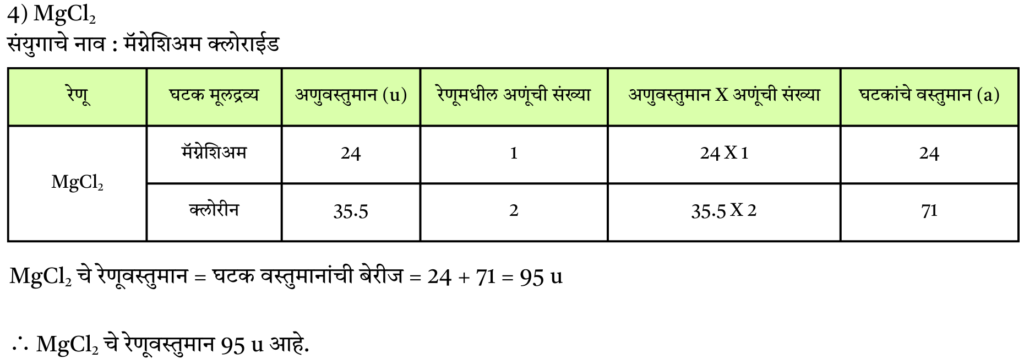
4) MgCl2
उत्तर :
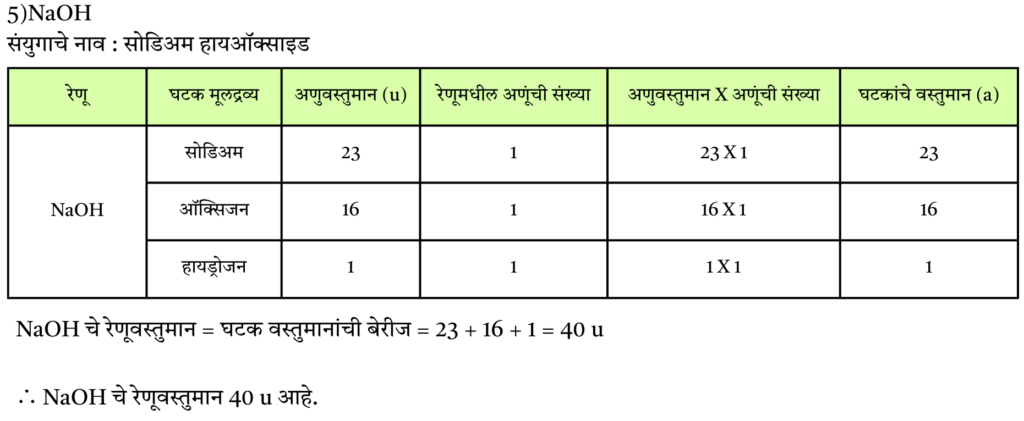
5) NaOH
उत्तर :
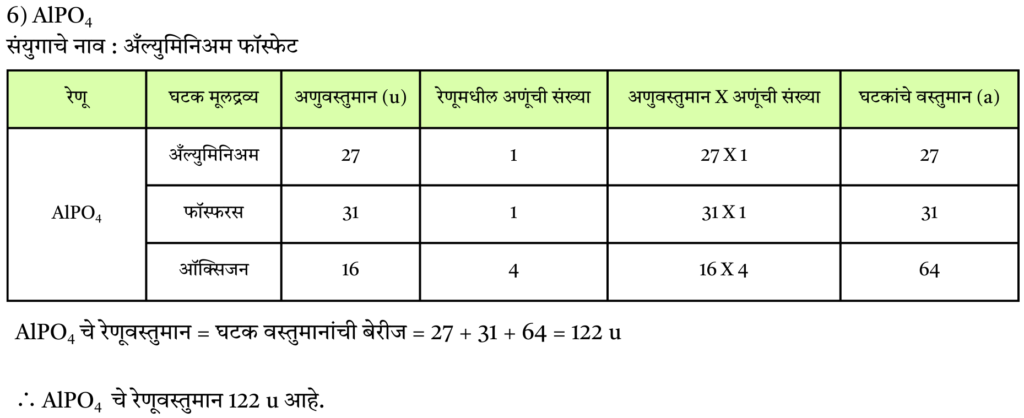
6) AlPO4
उत्तर :
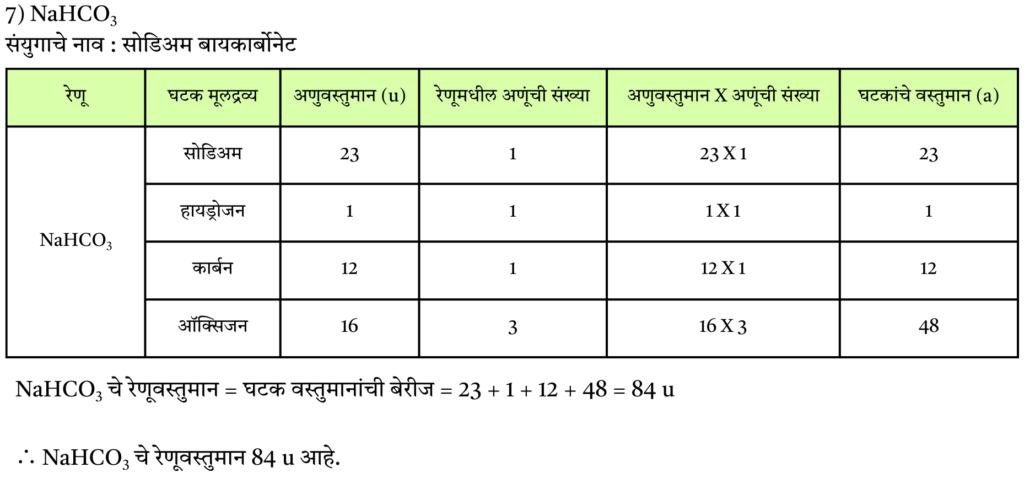
7) NaHCO3
उत्तर :
6. दोन वेगवेगळ्या मार्गानी चुनकळीचे ‘म’ आणि ‘न’ हे दोन नमुने मिळाले. त्यांच्या संघटनाचे तपशील पुढीलप्रमाणे :
‘नमुना म’ : वस्तुमान 7 ग्रॅम
घटक ऑक्सिजनचे वस्तुमान : 2 ग्रॅम
घटक कॅल्शियमचे वस्तुमान : 5 ग्रॅम
‘नमुना न’ वस्तुमान 1.4 ग्रॅम
घटक ऑक्सिजनचे वस्तुमान : 0.4 ग्रॅम
घटक कॅल्शियमचे वस्तुमान : 1 ग्रॅम
यावरून रासायनिक संयोगाचा कोणता नियम सिद्ध होतो ते स्पष्ट करा.
उत्तर :
1) नमुना ‘म’ : वस्तुमान 7 ग्रॅम
घटक ऑक्सिजनचे वस्तुमान : 2 ग्रॅम
घटक कॅल्शिअमचे वस्तुमान : 5 ग्रॅम
∴ ऑक्सिजन आणि कॅल्शिअम यांचे वजनी प्रमाण = 2 : 5
2) नमुना ‘न’ : वस्तुमान 1.4 ग्रॅम
घटक ऑक्सिजनचे वस्तुमान : 0.4 ग्रॅम
घटक कॅल्शिअमचे वस्तुमान : 1.0 ग्रॅम
∴ ऑक्सिजन आणि कॅल्शिअम यांचे वजनी प्रमाण = 0.4 : 1.0 = 2.5
3) चुनकळीच्या दोन्ही नमुन्यातील घटक मूलद्रव्यांचे वजनीप्रमाण स्थिर आहे.
4) यावरून स्थिर प्रमाणाचा नियम सिद्ध होतो.
7. खालील राशींमधील त्या त्या पदार्थाच्या रेणूंची संख्या काढा.
32 ग्रॅम ऑक्सिजन, 90 ग्रॅम पाणी, 8.8 ग्रॅम कार्बन डायऑक्साइड, 7.1 ग्रॅम क्लोरीन
उत्तर :
1) 32 ग्रॅम ऑक्सिजन
ऑक्सिजन (O2) रेणुवस्तुमान = 16 X 2 = 32
∴ 1 मोल ऑक्सिजन = 32 ग्रॅम ऑक्सिजन
तसेच,
1 मोल ऑक्सिजनमधील रेणूंची संख्या = 6.022 X 1023
∴ 32 ग्रॅम ऑक्सिजनमधील रेणूंची संख्या = 6.022 X 1023
2) 90 ग्रॅम पाणी
पाणी (H2O) रेणुवस्तुमान = (2X1) + 16 = 18
∴ 1 मोल पाणी = 18 ग्रॅम पाणी
∴ 90 ग्रॅम पाण्यामधील मोलची संख्या = 90/18 = 5 मोल
1 मोल पाण्यामधील रेणूंची संख्या = 6.022 X 1023
∴ 5 मोल पाण्यामधील रेणूंची संख्या = 5 X 6.022 X 1023
= 30.11 X 1023
= 3.01 X 1024
∴ 90 ग्रॅम पाण्यातील रेणूंची संख्या = 3.01 X 1024
3) 8.8 ग्रॅम कार्बन डायऑक्साइड
कार्बन डायऑक्साइड (CO2) चे रेणुवस्तुमान
= (12 X 1) + (16 X 2) = 44
∴ 1 मोल कार्बन डायऑक्साइड = 44 ग्रॅम कार्बन डायऑक्साइड
∴ 8.8 ग्रॅम कार्बन डायऑक्साइड मधील मोलची संख्या = 8.8/44 = 0.2 मोल
1 मोल कार्बन डायऑक्साइड मधील रेणूंची संख्या = 6.022 X 1023
∴ 0.2 मोल कार्बन डायऑक्साइड मधील रेणूंची संख्या = 0.2 X 6.022 X 1023
= 1.2044 X 1023
∴ 8.8 ग्रॅम कार्बन डायऑक्साइड मधील रेणूंची संख्या = 1.2044 X 1023
4) 7.1 ग्रॅम क्लोरीन
क्लोरीन (Cl2) चे रेणुवस्तुमान = (2 X 35.5) = 71
∴ 1 मोल क्लोरीन = 71 ग्रॅम क्लोरीन
∴ 7.1 ग्रॅम क्लोरीनमधील मोलची संख्या = 7.1/71
= 0.1 मोल
1 मोल क्लोरीनमधील रेणूंची संख्या = 6.022 X 1023
∴ 0.1 मोल क्लोरीनमधील रेणूंची संख्या = 0.1 X 6.022 X 1023
= 6.022 X 1022
∴ 7.1 ग्रॅम क्लोरीनमधील रेणूंची संख्या = 6.022 X 1022
8. खालील पदार्थाचे 0.2 मोल हवे असल्यास त्यांच्या किती ग्रॅम राशी घ्याव्या लागतील ?
सोडिअम क्लोराईड, मॅग्नेशिअम ऑक्साईड, कॅल्शिअम कार्बोनेट
उत्तर :
1) सोडिअम क्लोराईड
सोडिअम क्लोराईड (NaCl) रेणुवस्तुमान = 23 + 35/5 = 58.5
∴ 1 मोल सोडिअम क्लोराईड = 58.5 ग्रॅम सोडिअम क्लोराईड
ग्रॅममधील सोडिअम क्लोराईडचे वस्तुमान
= सोडिअम क्लोराईडच्या मोलची संख्या X रेणुवस्तुमान
= 0.2 X 58.5 = 11.7 ग्रॅम
∴ 0.2 मोल सोडिअम क्लोराईड = 11.7 ग्रॅम सोडिअम क्लोराईड
2) मॅग्नेशिअम ऑक्साईड
मॅग्नेशिअम ऑक्साईडचे (MgO) रेणुवस्तुमान = 24 + 16 = 40
∴ 1 मोल मॅग्नेशिअम ऑक्साईड = 40 ग्रॅम मॅग्नेशिअम ऑक्साईड
ग्रॅममधील मॅग्नेशिअम ऑक्साईडचे वस्तुमान
= मॅग्नेशिअम ऑक्साईडच्या मोलची संख्या X रेणुवस्तुमान
= 0.2 X 40 = 8.0 ग्रॅम
∴ 0.2 मोल मॅग्नेशिअम ऑक्साईड = 8.0 ग्रॅम मॅग्नेशिअम ऑक्साईड
3) कॅल्शिअम कार्बोनेट
कॅल्शिअम कार्बोनेटचे (CaCO3) रेणुवस्तुमान = 40 + 12 + 48 = 100
∴ 1 मोल कॅल्शिअम कार्बोनेट = 100 ग्रॅम कॅल्शिअम कार्बोनेट
ग्रॅममधील कॅल्शिअम कार्बोनेटचे वस्तुमान
= कॅल्शिअम कार्बोनेटच्या मोलची संख्या X रेणुवस्तुमान
= 0.2 X 100 = 20 ग्रॅम
∴ 0.2 कॅल्शिअम कार्बोनेट = 20 ग्रॅम कॅल्शिअम कार्बोनेट
