अणूचे अंतरंग स्वाध्याय
अणूचे अंतरंग स्वाध्याय इयत्ता आठवी सामान्य विज्ञान

1. खालील प्रश्नांची उत्तरे लिहा.
अ) थाॅमसन व रुदरफोर्ड यांच्या अणुप्रारूपांत कोणता फरक आहे ?
उत्तर :
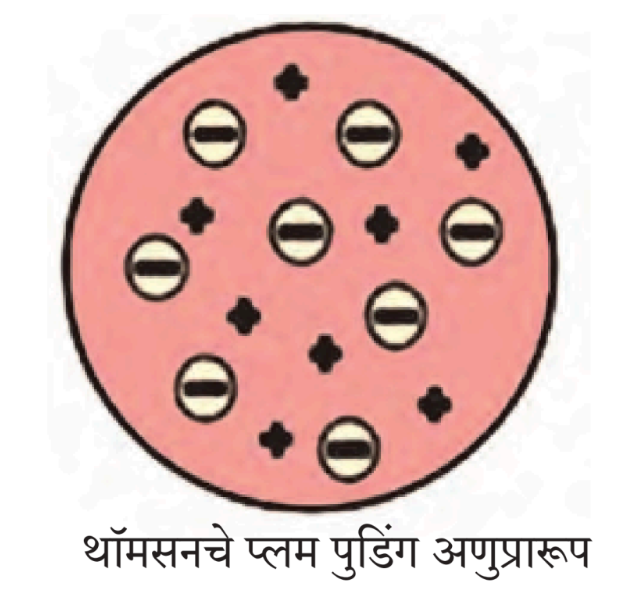
थाॅमसनचे अणूप्रारूप – थॉमसनने सुचविलेल्या अणुप्रारूपानुसार अणुच्या अंतरंगात धन व ऋण प्रभारित कण सर्वत्र पसरलेले असतात. ज्याप्रमाणे प्लम पुडिंगमध्ये सुकलेल्या फळाचे तुकडे असतात त्याप्रमाणे यात धन आणि ऋण प्रभारित कण सर्वत्र पसरलेले असतात. त्यांचे प्रमाण समान असते. त्यामुळे अणू विद्युतदृष्ट्या उदासिन आहे.
रुदरफोर्डचे अणूप्रारूप –
रुदरफोर्डने धन आणि ऋण प्रभारित कणांचे अस्तित्व मान्य केले पण त्यांची रचना मात्र थोडी वेगळी सुचविली आहे.
i) अणु मुख्यत: पोकळ असतो.
ii) त्याच्या मध्यभागी अणूचे वस्तुमान एकवटले असते. त्याला केंद्रक म्हणतात.
iii) अणू केंद्रक धन प्रभारित असते.
iv) अणू केंद्रकाभोवताल ऋणप्रभारित कण परिभ्रमण करीत असतात.
v) धन आणि ऋण कणांची संख्या सारखी असते. त्यामुळे अणु विद्युतदृष्ट्या उदासिन असतो.
आ) मूलद्रव्यांची संयुजा म्हणजे काय ? संयुजा इलेक्ट्रॉन संख्या व संयुजा यांच्यातील संबंध काय ते लिहा.
उत्तर :
अणू आपल्या बाह्यतम कवचातील इलेक्ट्रॉन वापरुन रासायनिक बंध तयार करतो. मूलद्रव्याची संयुजा म्हणजे त्याच्या एका अणूने तयार केलेल्या रासायनिक बंधांची संख्या.
उदा. i) Na चे अणू संरुपण (2,8,1) आहे. ह्याचा अणू त्याच्या बाह्यतम कवचातील एक इलेक्ट्रॉन वापरून एक रासायनिक बंध तयार करतो म्हणून त्याची संयुजा एक आहे.
उदा. ii) Cl (2,8,7) क्लोरीन ह्या मूलद्रव्याचा अणू त्याच्या बाह्यतम कक्षेतील इलेक्ट्रॉनचा वापर करून एकच रासायनिक बंध तयार करतो. कारण त्यामुळे त्याची अष्टक स्थिती पूर्ण होते. अर्थात क्लोरीनची संयुजा एक आहे व अष्टक स्थिती पूर्ण करण्यास एक इलेक्ट्रॉन कमी पडतो.
संयुजा व संयुजा इलेक्ट्रॉन यातील संबंध
i) संयुजा इलेक्ट्रॉनची संख्या 4 किंवा 4 पेक्षा कमी असल्यास
संयुजा = संयुजा इलेक्ट्रॉनची संख्या
ii) संयुजा इलेक्ट्रॉनची संख्या 4 पेक्षा जास्त असल्यास
संयुजा = 8 – संयुजा इलेक्ट्रॉनची संख्या
इ) अणुवस्तुमानांक म्हणजे काय ? कार्बनचा अणुअंक 6 तर अणुवस्तुमानांक 12 आहे. हे कसे ते स्पष्ट करा.
उत्तर :
अणुवस्तुमानांक – मूलद्रव्याच्या अणुतील प्रोटॉन व न्यूट्रॉन यांची एकत्रित संख्या म्हणजे अणुवस्तुमानांक होय.
अणुअंक – मूलद्रव्यांच्या अणुमधील प्रोटॉनची संख्या म्हणजे त्या मूलद्रव्याचा अणुअंक होय.
उदा. कार्बन मधील अवअणुकण
इलेक्ट्रॉन = 6
प्रोट्रॉन = 6
न्यूट्रॉन = 6
∴ अणुअंक = प्रोट्रॉनची संख्या = 6
अणुवस्तुमानांक = (प्रोट्रॉन + न्यूट्रॉन) ची संख्या
= 6 + 6
= 12
ई) अवअणुकण म्हणजे काय ? विद्युतप्रभा, वस्तुमान व स्थान ह्या संदर्भात तीन अवअणुकणांची थोडक्यात माहिती लिहा.
उत्तर :
अणूंना अंतर्गत संरचना असते. त्यात अनेक प्रकारचे लहान लहान कण असतात. त्यांना अवअणुकण म्हणतात. इलेक्ट्रॉन, प्रोट्रॉन व न्यूट्रॉन हे तीन महत्त्वाचे अवअणुकण आहेत.
प्रोट्रॉन – हे धन प्रभारित कण अणुच्या केंद्रकात असतात. त्यांच्या वरील प्रभार +1e एवढा असतो. त्याचे वस्तुमान सुमारे 1u असते.
इलेक्ट्रॉन – हे ऋणप्रभारित अवअणुकण केंद्रकामधील परिभ्रमण करीत असतात. त्यांच्या वरील प्रभार -1e त्यांचे वस्तुमान प्रोट्रॉनच्या वस्तूमानाच्या 1/1800 पट असते.
न्यूट्रॉन – हे प्रभार नसलेले अवअणुकण अणू केंद्रकात असतात. त्यांच्या वरील प्रभार शून्य असतो. त्यांचे वस्तुमान सुमारे 1u असते.
2. शास्त्रीय कारणे लिहा.
अ. अणूचे सगळे वस्तुमान केंद्रकात एकवटलेले असते.
उत्तर :
कारण मुख्य अवअणुकण तीन प्रकारचे असतात. इलेक्ट्रॉन, प्रोट्रॉन व न्यूट्रॉन यापैकी, इलेक्ट्रॉनची वस्तुमान नगण्य असून प्रोट्रॉन व न्यूट्रॉनला मात्र वस्तुमान सुमारे 1u आहे. हे दोन्ही वस्तुमान असणारे कण अणुकेंद्रकात असतात त्यामुळे अणूचे वस्तुमान केंद्रकात एकवटलेले असते.
आ. अणू विद्युतदृष्ट्या उदासीन असतो.
उत्तर :
कारण प्रभार असणारे अवअणुकण दोन असतात. ते प्रोटॉन व इलेक्ट्रॉन आहे.
प्रोट्रॉनवर धन प्रभार व इलेक्ट्रॉनवर ऋण प्रभार असतो. त्यांची संख्या समान असते. त्यामुळे एकूण धन व ऋण प्रभार समान झाल्यामुळे अणू विद्युतदृष्ट्या उदासिन असतो.
इ. अणुवस्तुमानांक पुर्णाकात असते.
उत्तर :
i) अणूमधील प्रोटॉन व न्यूट्रॉन यांच्या एकत्रित संख्येला त्या मूलद्रव्याचा अणुवस्तुमानांक म्हणतात.
ii) प्रोटॉन व न्यूट्रॉन पूर्णाकात असल्यानेच अणुवस्तुमानांक सुद्धा पूर्णाकात असते.
ई. परिभ्रमण करणारे प्रभारित इलेक्ट्रॉन असूनही सामान्यपणे अणूंना स्थायीभाव असतो.
उत्तर :
कारण इलेक्ट्रॉनवर ऋण प्रभार असून ते केंद्रकाभोवती भ्रमण करीत असतात. त्यामुळे त्यांची ऊर्जा कमी कमी होत जाऊन इलेक्ट्रॉन केंद्रकावर कोसळतील व अणू अस्थायी होईल. असे भौतिक शास्त्रातील नियम सांगतो. पण तसे होत नाही याचे कारण रूदरफोर्डच्या अणुप्रारूपातील ही त्रूटी नील्स बोर यांनी मांडलेल्या अणुप्रारूपाने दूर झाली.
बोरच्या अणुप्रारूपातील मूलतत्त्वे खालीलप्रमाणे आहेत.
i) इलेक्ट्रॉन, केंद्रकाभोवती, केंद्रकापासून विशिष्ट अंतरावर असणाऱ्या समकेंद्री वर्तुळावर कक्षांमध्ये फिरत असतात.
ii) एकाच कक्षेत फिरतांना त्याची ऊर्जा स्थिर असते.
iii) इलेक्ट्रॉन एका कक्षेतून दुसऱ्या कक्षेत उडी मारतात. आतील कक्षेत उडी मारताना ऊर्जा उत्सर्जित करतात तर बाहेरील कक्षेत उडी मारतात ऊर्जा शोषण करतात. त्यामुळे अणुप्रारूपाला स्थायीभाव प्राप्त होतो.
3. व्याख्या लिहा.
1. अणू
उत्तर :
रासायनिक संयोगात भाग घेणारा मूलद्रव्याचा लहानात लहान कण म्हणजे अणू होय.
2. समस्थानिके
उत्तर :
मूलद्रव्यामध्ये अणुअंक समान पण अणुवस्तुमानांक मात्र भिन्न असे अणू असतात त्यांना समस्थानिके म्हणतात.
उदा. क्लोरीनची समस्थानिके 3517Cl व 3717Cl यात अणुअंक 17 आहे. पण अणुवस्तुमानांक मात्र 35 व 37 असे भिन्न भिन्न आहेत.
3. अणुअंक
उत्तर :
मूलद्रव्याच्या अणुतील प्रोट्रॉनची संख्या म्हणजे त्या मूलद्रव्याचा अणुअंक होय.
4. अणुवस्तुमानांक
उत्तर :
मूलद्रव्याच्या अणुतील प्रोट्रॉन व न्यूट्रॉनच्या एकत्रित बेरजेला त्या मूलद्रव्याचा अणुवस्तुमानांक म्हणतात.
5. अणुभट्टीतील मंदक
उत्तर :
अणुभट्टीत न्यूट्रॉनचा मारा करून शृंखला अभिक्रिया घडवून आणतात. शृंखला अभिक्रिया नियंत्रित करण्यासाठी न्यूट्रॉनचा वेग कमी जास्त करावा लागतो. त्यासाठी ग्राफाइड किंवा जड पाणी वापरतात. त्यांना मंदक म्हणतात.
4. सुबक व नामनिर्देशित आकृती काढा.
अ. रुदरफोर्डचा विकीरण प्रयोग
उत्तर :
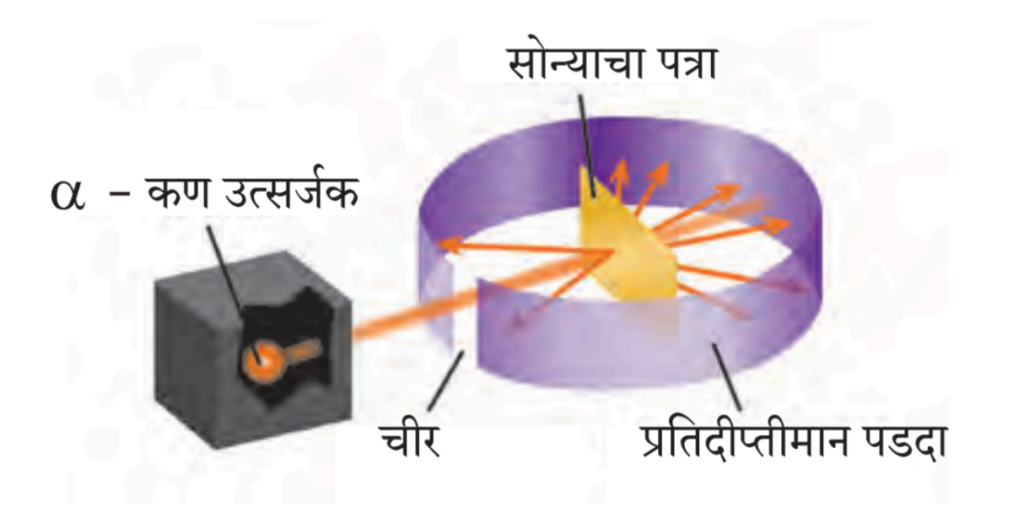
आ. थॉमसनचे अणुप्रारूप
उत्तर :
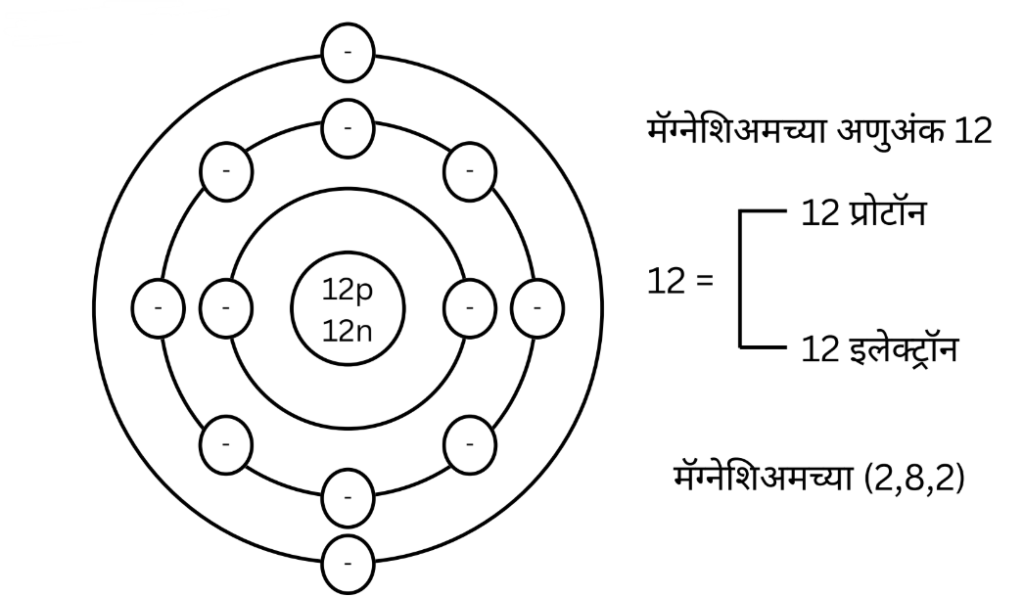
इ. मॅग्नेशिअमच्या (अणुअंक 12) इलेक्ट्रॉन संरूपणाचे रेखाटन
उत्तर :
ई. अँरगॉनच्या (अणुअंक 18) इलेक्ट्रॉन संरूपणाचे रेखाटन
उत्तर :
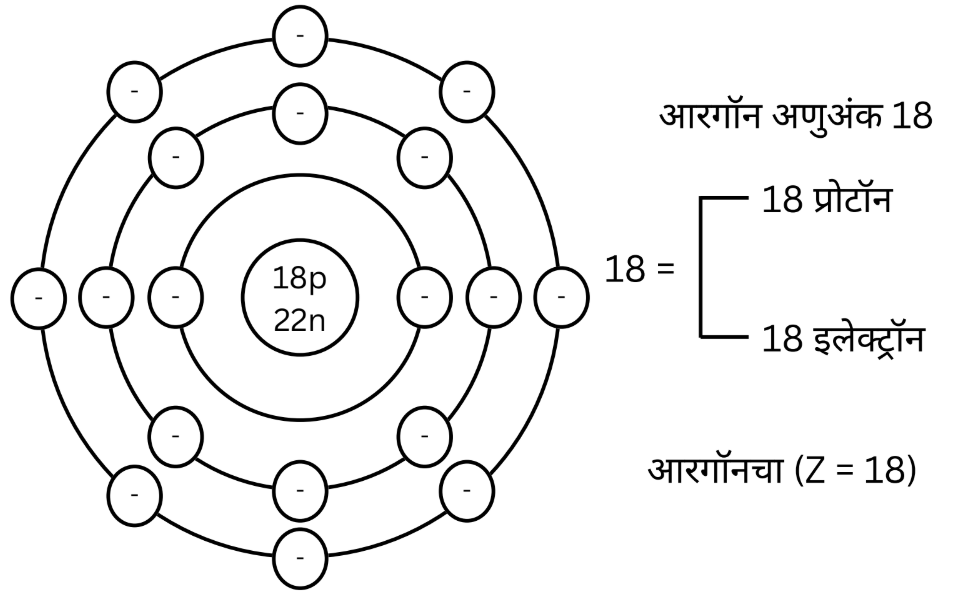
5. रिकाम्या जागा भरा.
अ. इलेक्ट्रॉन, प्रोट्रॉन, न्यूट्रॉन हे अणुमध्ये असणारे ……………….. आहेत.
उत्तर :
इलेक्ट्रॉन, प्रोट्रॉन, न्यूट्रॉन हे अणुमध्ये असणारे अवअणुकण आहेत.
आ. इलेक्ट्रॉनवर ……………….. प्रभार असतो.
उत्तर :
इलेक्ट्रॉनवर ऋण प्रभार असतो.
इ. अणुकेंद्रकापासून सर्वात जवळचे इलेक्ट्रॉन कवच …………………. हे आहे.
उत्तर :
अणुकेंद्रकापासून सर्वात जवळचे इलेक्ट्रॉन कवच K हे आहे.
ई. मॅग्नेशिअमचे इलेक्ट्रॉन संरूपण 2,8,2 आहे. यावरून असे समजते की मॅग्नेशिअमचे संयुजा कवच …………………… हे आहे.
उत्तर :
मॅग्नेशिअमचे इलेक्ट्रॉन संरूपण 2,8,2 आहे. यावरून असे समजते की मॅग्नेशिअमचे संयुजा कवच M हे आहे.
उ. H2O ह्या रेणूसूत्रानुसार हयड्रोजनची संयुजा 1 आहे. त्यामुळे Fe2O3 ह्या सूत्रानुसार Fe ची संयुजा ………………….. ठरते.
उत्तर :
H2O ह्या रेणूसूत्रानुसार हयड्रोजनची संयुजा 1 आहे. त्यामुळे Fe2O3 ह्या सूत्रानुसार Fe ची संयुजा तीन ठरते.
6. जोड्या जुळवा.
| ‘अ’ गट | ‘ब’ गट |
|---|---|
| अ. प्रोट्रॉन | i. ऋणप्रभारित |
| आ. इलेक्ट्रॉन | ii. उदासीन |
| इ. न्यूट्रॉन | iii. धनप्रभारित |
उत्तर :
| ‘अ’ गट | ‘ब’ गट |
|---|---|
| अ. प्रोट्रॉन | iii. धनप्रभारित |
| आ. इलेक्ट्रॉन | i. ऋणप्रभारित |
| इ. न्यूट्रॉन | ii. उदासीन |
7. दिलेल्या माहितीवरून शोधून काढा.
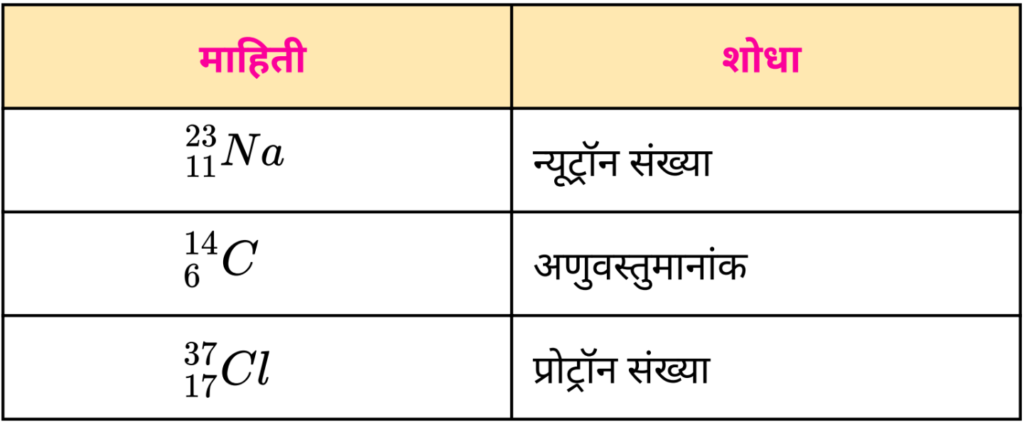
उत्तर :
i) न्यूट्रॉनची संख्या = A – Z
= 23 – 11
= 12
ii) अणुवस्तुमानांकाची संख्या = A
= 14
iii) प्रोट्रॉनची संख्या = Z
= 17
